Nyílt szénhidrogén
| Szén | Képlet | Név | Sav | Acil[1] |
|---|---|---|---|---|
| 1 | CH4 | + metán karbán |
× hangyasav | form-[2] |
| 2 | CH3–CH3 | + etán[3] | + ecetsav | acet- |
| × glikolsav | glikol- | |||
| × glioxilsav oxo-ecetsav |
glioxil- oxo-acet- | |||
| × oxálsav | oxal- | |||
| CH2═CH2 | etén[4] | |||
| CH≡CH | + acetilén | |||
| 3 | CH3–CH2–CH3 | + propán | × propionsav propánsav |
propion- |
| + malonsav propándisav |
malon- | |||
| × tejsav | lakt- | |||
| × glicerinsav | glicer- | |||
| × piroszőlősav | piruv- | |||
| CH3–CH═CH2 | propén[5] |
+ akrilsav | akril- | |
| CH3–C≡CH | propin metilacetilén |
× propiolsav | propiol- | |
| 4 | CH3–[CH2]2–CH3 | + bután | × vajsav butánsav |
butir- |
| + borostyánkősav | szukcin- | |||
| × acetecetsav | acetoecet- | |||
| × borkősav | tartar- | |||
| (CH3)2CH–CH3 | × izobután | × izovajsav izobutánsav |
izobutir- | |
| (CH3)2C═CH2 | × izobutén | × metakrilsav | metakril- | |
| CH3–CH═CH–CH3 | 2-butén | × fumársav | fumar- | |
| × maleinsav | male- | |||
| ||||
Az alkánok telítettek, az alkének és alkinek telítetlenek.
Nyílt, telített, egyenes láncú szénhidrogének
A nyílt, telített, egyenes láncú szénhidrogének alapvegyületek. Az első négy ilyen szénhidrogén neve (jobb oldali táblázat):
- metán
- etán
- propán
- bután
A nagyobb szénatomszámú szénhidrogének nevét a görög számokból képezzük úgy, hogy a szó végi -a-t „-án”-ra cseréljük. A láncot az egyik végétől kezdve megszámozzuk.
Példák:
- hexán (6 szénatom): CH3–[CH2]4–CH3
- trikozán (23 szénatom): CH3–[CH2]21–CH3
Nyílt szénhidrogének
Az elágazó láncok elnevezésének első lépése a (nem elágazó) főlánc megállapítása.[Erdey 1]
- a főlánc a lehető legtöbb telítetlen kötést tartalmazza
- az előző pontbeliek közül a leghosszabb
- az előző pontbeliek közül a legtöbb kettős kötést tartalmazza
A láncot úgy számozzuk meg, hogy a kettős és hármas kötések a lehető legkisebb számokat kapják, több lehetőség esetén pedig a kettős kötés kapja a kisebb helyszámot. Ha a fenti három pont sem ad eredményt, a változatok közül a számozás alapján döntünk.
Ezután minden oldalláncnál ugyanígy járunk el (rekurzió). A végül kapott egyenes láncból szubtraktív művelettel (leggyakrabban az -il utótaggal) gyököt képzünk. Az oldallánc számozása attól függ majd, hogy az ottani két lehetőség közül melyiket választjuk. Az így kapott gyököket szubsztitúcióval kapcsoljuk a főlánchoz.
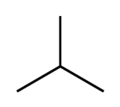
Példa: izobután
|
A főlánc a propán (CH3–CH2–CH3). Ez az alapnév, melyhez a 2-es (középső) szénatomon csatlakozik egy metilcsoportból álló oldallánc.
A metán (CH4) és propán két nyílt, telített, egyenes láncú szénhidrogén triviális neve. A metil (CH3–) a metánból szubtrakcióval képzett név, melyet előtagként adunk meg a névben. A két nevet szubsztitúcióval kapcsoljuk össze: a propán középső szénatomjából eltávolítunk egy hidrogént, és összeillesztjük a két láncot. Az elnevezési szabályok szerint az utolsó előtagot egybeírjuk az alapnévvel. Az izobután egyik rendszertani neve így 2-metilpropán. Az izobután ugyancsak rendszertani, féltriviális név.
|
Jegyzetek
- ↑ A triviális nevű sav töve a sav latin nevének töve, amiből a rokon vegyületek nevét képezzük (aldehidek, aminok, nitrilek, stb.).
- ↑ Sav anionja a -formiát
- ↑ Kétértékű szubsztituense az etilén: –CH2–CH2–.
- ↑ Egyértékű szubsztituense a vinil: CH2═CH–.
- ↑ Egyértékű szubsztituense az allil: CH2═CH–CH2–.
Forrás
- A magyar kémiai elnevezés és helyesírás szabályai. Szerkesztette: Erdey-Grúz Tibor és Fodorné Csányi Piroska Budapest: Akadémiai Kiadó (1972)
- ↑ A-3.4.
- Nyitrai József – Nagy József: Útmutató a szerves vegyületek IUPAC nevezéktanához. Budapest: Magyar Kémikusok Egyesülete (1998) Az IUPAC Szerves Kémiai Nómenklatúrabizottságának 1993-as ajánlása alapján.
- ↑ R-9.1., 19. és 28. táblázat, 172. és 184. oldal.